LCC
L’utilisation des complexes RuNO dans les tissus biologiques pose la question délicate de leur mise en forme (molécules dispersées en solution, greffées sur des nanoparticules, des dendrimères ou des polymères, insérées dans des structures micellaires, …). L’obtention de ces objets offre plusieurs avantages car, au contraire des molécules isolées en solution qui ne peuvent pénétrer dans les cellules que par diffusion, ces objets peuvent être capturés par les cellules par des mécanismes beaucoup plus efficaces (ex. phagocytose) qui conduisent à un double effet :
- pénétration accrue des porteurs de NO,
- libération de multiples unités NO présentes dans la particule porteuse.
Nanoparticules de complexes nitrosyles du ruthénium
(Chem. Phys. Lett., 2023, 818, 140434)
Nous avons montré qu’il était possible d’obtenir des agrégats nanométriques du complexe trans(Cl,Cl)-[RuFTCl2NO]PF6 (FT : fluorényle) par précipitation contrôlée en solution aqueuse (Figure 1). Le diamètre moyen des nanoparticules dépend des conditions expérimentales, notamment de la vitesse d’ajout de la solution du complexe RuNO dans la phase aqueuse. Le rendement quantique de photo-libération (ΦNO) des nano-agrégats est de l’ordre de 0.12 (irradiation à 365 ou 400 nm). Il est indépendant de leur taille et de leur état de dispersion. Le rendement quantique des nanoparticules est tout à fait similaire à celui du même complexe sous forme de molécules isolées en solution. Ces nano-objets moléculaires peuvent alors être considérés comme une nano-plateforme de libération du NO pour la lutte antibactérienne.

Figure 1 : Image AFM de nano-agrégats du complexe trans(Cl,Cl)-[RuFTCl2NO]PF6 dispersés dans l’eau (diamètre moyen : 16 nm)
Complexes nitrosyles du ruthénium incorporés dans un hydrogel
(New J. Chem., 2024, 48, 8343)
Un hydrogel est un gel dans lequel l’agent gonflant est de l’eau. Les hydrogels dérivés du Pluronic F127 (PL) sont susceptibles de former spontanément des micelles dans l’eau. Leur organisation conduit à l’obtention d’un gel dans le domaine 20-40°C, compatible avec des applications médicales. Parfaitement biocompatibles et non toxiques, ils souffrent toutefois d’une faible tenue mécanique. Celle-ci peut être fortement améliorée par l’ajout de chitosane (CS) qui favorise le phénomène de réticulation. Ce sont ces hydrogels PL/CS que nous avons utilisés comme support d’incorporation d’un complexe RuNO.
Nous avons réalisé l’incorporation du complexe hydrosoluble trans(Cl,Cl)-[RuFTCl2NO]Cl dans des hydrogels PL/CS pour une teneur en RuNO de 13 à 520 µg.g‒1 sans observer de démixtion (Figure 2). Les hydrogels montrent une transition sol-gel entre 35 et 40°C selon la teneur en complexe RuNO (35°C pour l’hydrogel sans RuNO). Elle est donc peu modifiée par l’incorporation et la concentration du complexe, ce qui permet d’envisager des applications cutanées. Sous irradiation à 400 nm et à la température physiologique (37°C), les hydrogels hybrides PL/CS/RuNO sont susceptibles de libérer le monoxyde d’azote comme cela a été montré par résonance paramagnétique électronique (Figure 3) et par détection électrochimique (capteur sensible à NO). Le rendement quantique de photo-libération (ΦNO) est de 0.014 (à 37°C pour une irradiation à 400nm).

Figure 2 : Image AFM d’un hydrogel PL/CS incorporant le complexe trans(Cl,Cl)-[RuFTCl2NO]Cl (13 µg.g‒1)
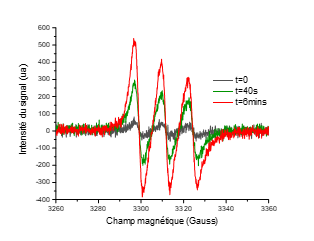
Figure 3 : Mise en évidence par RPE de la libération de NO pour un hydrogel hydrogel PL/CS incorporant le complexe trans(Cl,Cl)-[RuFTCl2NO]Cl (13 µg.g‒1)
Nanoparticules de platine fonctionnalisées par un complexe nitrosyle du ruthénium
Des quantums dots de graphène ou de sulfures de métaux du groupe 12 fonctionnalisés par des complexes RuNO sont bien décrits dans la bibliographie. En revanche, la fonctionnalisation de nanoparticules métalliques par un dérivé RuNO n’a pas encore été décrite à notre connaissance.
Nous avons préparé les premières nanoparticules métalliques fonctionnalisées par un dérivé nitrosyle du ruthénium. Des nanoparticules de platine de formule générale Ptx(CO)y(CH3CN)z, élaborées dans l’équipe de Simon Tricard au LPCNO de Toulouse, ont été dispersées dans l’acétonitrile et mises en présence du complexe trans(Cl,Cl)-[RuTTCl2NO]PF6 (Figure 4).
La substitution de certains ligands CH3CN et/ou CO par le groupement thiophène du ligand terpyridine du complexe RuNO a été mise en évidence par spectroscopie infrarouge. Les nanoparticules de platine ainsi fonctionnalisées, de formule postulée Ptx’(CO)y’(CH3CN)z’(RuNO)t, se regroupent en agrégats dans lesquels la taille des particules individuelles est de 1 à 3 nm (Figure 5).
Les caractéristiques courant-tension des nanoparticules montrent un blocage de Coulomb supérieur à celui de Ptx(CO)y(CH3CN)z, en accord avec l’introduction d’une barrière moléculaire supplémentaire à l’interface et une réduction des couplages électroniques entre nanoparticules adjacentes. Finalement, la RPE met en évidence la photo-libération de NO sous irradiation à 365 nm des nano-objets Ptx’(CO)y’(CH3CN)z’(RuNO)t. Nous étudions actuellement l’influence de l’excitation plasmon sur l’efficacité de libération du monoxyde d’azote en solution.
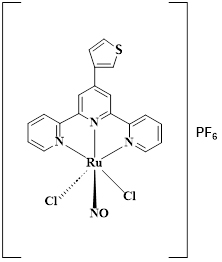
Figure 4 : Formule du complexe trans(Cl,Cl)-[RuTTCl2NO]PF6
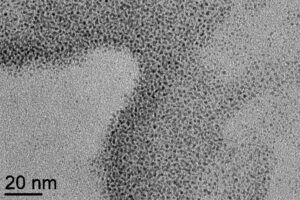
Figure 5 : Image de microscopie électronique à transmission de nanoparticules de platine fonctionnalisées par le complexe trans(Cl,Cl)-[RuTTCl2NO]PF6
LCC CNRS
Laboratoire de chimie de coordination du CNRS
205 route de Narbonne, BP 44099
31077 Toulouse cedex 4
France




