LCC
Ces vingt dernières années, la résistance aux antibiotiques de nombreux pathogènes, notamment ceux impliqués dans les maladies nosocomiales est en recrudescence. En 2016, Margaret Chan, directrice générale de l’Organisation Mondiale de la Santé a qualifié cette résistance de « crise planétaire, aujourd’hui reconnue comme une des plus importantes menaces sur la santé ».
Les souches de Staphylococcus epidermidis font partie des bactéries les plus souvent impliquées dans les infections chez l’homme. S. epidermidis est en général la cause la plus importante d’infections, et la deuxième cause d’infections liées à l’implantation d’un dispositif médical.
Ces bactéries sont en effet capables de s’accumuler dans un biofilm hydrophobe qui adhère à des surfaces telles que les dispositifs médicaux. Souvent ces infections deviennent chroniques car le système immunitaire ne parvient pas à se débarrasser de ces microorganismes.
Devant les difficultés rencontrées par les antibiotiques usuels pour traiter certaines infections et particulièrement celles dues aux biofilms, il est urgent de développer de nouvelles thérapies qui permettraient de lutter contre la résistance antimicrobienne.
Le monoxyde d’azote présente des propriétés bactéricides, il est notamment décrit comme pouvant induire la dispersion de biofilms bactériens.
Les complexes de ruthénium à ligand nitrosyle sont donc de potentiels agents antimicrobiens.
La libération contrôlée de l’agent bactéricide par la lumière permet d’imaginer de nouvelles thérapies ciblées et contrôlées.
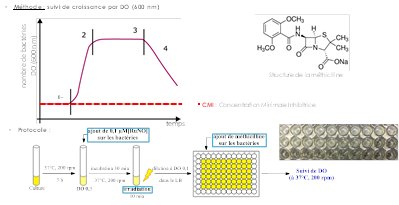
Figure 1 : Protocole mis au point dans l’évaluation de l’effet bactéricide des complexes de ruthénium à ligand nitrosyle
(collaboration M.-P. Rols, IPBS, Toulouse, P. Vicendo, IMRCP, Toulouse)
La souche de Staphylococcus epidermidis ATCC 35984 est résistante à la méthicilline et est capable de former des agrégats et des biofilms. Le complexe trans (NO,OH)-[RuFT(Cl)(OH)(NO)]PF6 a été testé sur cette souche et ne présente pas de toxicité sans irradiation.
Au contraire, l’utilisation de 0,1 µM de complexe et l’irradiation des bactéries traitées font chuter la viabilité des deux souches d’environ 50 %.
La combinaison de ce donneur de NO• avec la méthicilline a ensuite été étudiée. Après traitement des bactéries par le complexe trans (NO,OH)-[RuFT(Cl)( OH)(NO)]PF6 et irradiation, les concentrations minimales inhibitrices de la méthicilline chutent d’un facteur 100, ce qui constitue un résultat majeur.
Les complexes de ruthénium à ligand nitrosyle sont donc des candidats prometteurs dans la lutte contre la résistance bactérienne.
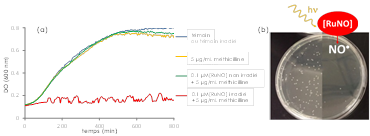
Figure 2 : trans (NO,OH)-[RuFT(Cl)(OH)NO]+ et Staphylococcus epidermidis ATCC 35984:
Evolution de la croissance bactérienne (a); colonies bactériennes sans (à gauche) et (b) avec traitement (à droite) antibiotique.
LCC CNRS
Laboratoire de chimie de coordination du CNRS
205 route de Narbonne, BP 44099
31077 Toulouse cedex 4
France




